Introdução – o gelo, o vapor e a pergunta que sempre aparece em prova
Você já parou para pensar por que um cubo de gelo mantém sua forma quando está sobre a mesa, mas a água escorre imediatamente quando ele derrete? Ou por que o vapor que sai de uma panela com água quente “desaparece” no ar, enquanto o óleo nunca se comporta da mesma maneira? Essas situações fazem parte do nosso cotidiano e, ao mesmo tempo, escondem um dos conteúdos mais recorrentes da Química no Ensino Médio: os estados físicos da matéria.
Esse tema aparece com frequência em vestibulares porque ele conecta conceitos microscópicos, como o comportamento das partículas, com fenômenos macroscópicos que observamos todos os dias. Além disso, os estados físicos são fundamentais para entender mudanças de estado, separação de misturas, transformações físicas e até processos industriais e ambientais.
No ENEM, esse conteúdo costuma aparecer contextualizado, ligado a situações do dia a dia, gráficos ou problemas ambientais. Em vestibulares tradicionais, como Fuvest e Unicamp, a cobrança é mais conceitual, exigindo clareza na definição e comparação entre os estados. Já em provas militares, o rigor é maior: espera-se precisão, domínio de diagramas e compreensão profunda do comportamento molecular.
Neste texto, você vai aprender o que define cada estado físico da matéria, por que eles existem, como as partículas se organizam em cada caso e como identificar corretamente o que a questão está pedindo. Ao longo do caminho, vamos resolver exemplos típicos de prova e mostrar onde muitos alunos erram.
Este post dá continuidade direta ao conteúdo apresentado em “Matéria e suas transformações”. Se ainda restar alguma dúvida sobre classificação da matéria, sistemas e fases, vale a pena revisitar aquele texto antes de seguir.

O que são estados físicos da matéria
Estados físicos da matéria são formas distintas pelas quais a matéria pode se apresentar, dependendo das condições de temperatura e pressão. Mais do que aparência, o que diferencia um estado físico de outro é o modo como as partículas estão organizadas e como interagem entre si.
Toda matéria é formada por partículas que estão em constante movimento. A diferença é que, em alguns casos, esse movimento é mais intenso; em outros, mais limitado. Além disso, a distância entre as partículas e a intensidade das forças de atração entre elas também variam.
É justamente esse conjunto de fatores que determina se uma substância estará no estado sólido, líquido ou gasoso.
O estado sólido: forma e volume definidos
No estado sólido, as partículas estão muito próximas umas das outras e fortemente ligadas. Elas não estão paradas, como muitos imaginam, mas vibram em torno de posições fixas. Essa organização explica por que os sólidos possuem forma e volume definidos.
Um exemplo cotidiano é uma pedra, um livro ou um cubo de gelo retirado do congelador. Mesmo fora do recipiente, esses materiais mantêm sua forma.
Do ponto de vista microscópico, as forças de atração entre as partículas são intensas, o que limita o movimento. Isso torna os sólidos pouco compressíveis e relativamente rígidos.
Como isso aparece no ENEM: normalmente associado a situações do cotidiano, como gelo, metais, construção civil ou conservação de alimentos, exigindo interpretação conceitual.
Vestibulares tradicionais cobram assim: definição clara do estado sólido, comparação com outros estados e explicação do comportamento das partículas.
Atenção em provas militares: pode aparecer associado a modelos cristalinos, organização molecular e análise de gráficos de energia.

O estado líquido: volume definido, forma variável
No estado líquido, as partículas continuam próximas, mas com maior liberdade de movimento. Elas deslizam umas sobre as outras, o que permite que o líquido assuma a forma do recipiente, mas mantenha volume definido.
A água em um copo é o exemplo mais clássico. Se você trocar o copo por uma garrafa, a forma muda, mas a quantidade de água permanece a mesma.
Microscopicamente, as forças de atração ainda existem, mas são menos intensas do que no estado sólido. Isso explica por que líquidos escoam, mas não se expandem indefinidamente.
Erro comum de prova: achar que líquidos não possuem organização. Eles possuem, apenas menos rígida do que nos sólidos.

O estado gasoso: forma e volume variáveis
No estado gasoso, as partículas estão muito afastadas umas das outras e se movem livremente em todas as direções. As forças de atração entre elas são praticamente desprezíveis.
Isso faz com que os gases não tenham forma nem volume definidos. Eles ocupam todo o espaço disponível do recipiente e são facilmente compressíveis.
O ar que respiramos é um exemplo de mistura gasosa. O vapor de água que se espalha pelo ambiente após uma panela ferver é outro exemplo clássico.
Como cai em vestibulares: comparação entre compressibilidade, densidade e movimento das partículas.
Atenção em provas militares: uso de equações, análise de gráficos pressão versus volume e interpretação rigorosa.

Mudanças de estado físico
Quando a matéria passa de um estado físico para outro sem alterar sua composição química, ocorre uma transformação física. Essas mudanças estão associadas à absorção ou liberação de energia, geralmente na forma de calor.
As principais mudanças de estado são fusão, solidificação, vaporização, condensação e sublimação. Cada uma delas corresponde a uma transição específica entre estados físicos.
Por exemplo, quando o gelo derrete, ocorre a fusão, passando do estado sólido para o líquido. Quando a água ferve, ocorre a vaporização, passando do líquido para o gasoso.
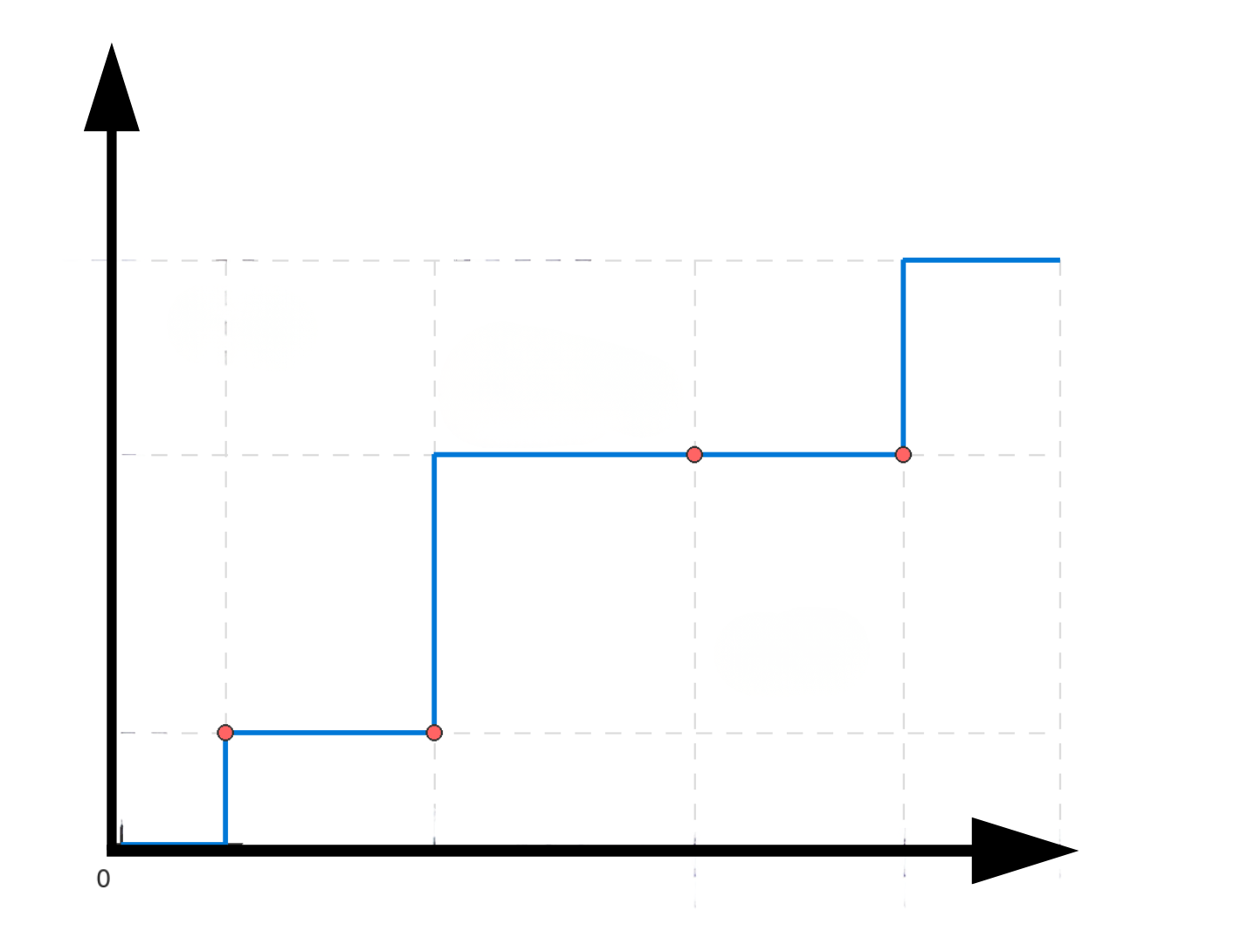
Esses processos são frequentemente cobrados em gráficos de aquecimento e resfriamento, onde a temperatura permanece constante durante a mudança de estado.
Exemplo resolvido – nível básico
Questão: Ao derreter um cubo de gelo em temperatura ambiente, ocorre uma transformação física porque
a) há formação de novas substâncias
b) ocorre mudança na composição química
c) apenas o estado físico da matéria é alterado
d) há liberação de gás durante o processo
O que a questão pede: identificar o tipo de transformação envolvida.
Resolução: o gelo e a água líquida possuem a mesma composição química, H₂O. O que muda é apenas o estado físico, de sólido para líquido.
Resposta: alternativa c.
Exemplo resolvido – nível intermediário
Questão: Em um experimento, um estudante aquece água até observar a formação de vapor. Durante a ebulição, a temperatura da água permanece constante. Isso ocorre porque
Resolução: durante a mudança de estado, a energia fornecida é utilizada para vencer as forças de atração entre as partículas, e não para aumentar a temperatura.
Esse tipo de questão aparece frequentemente no ENEM e em vestibulares tradicionais.
Links internos sugeridos
Para revisar os conceitos básicos que fundamentam este conteúdo, acesse o post “Matéria e suas transformações”.
Para aprofundar o estudo, veja também:
Separação de misturas
Transformações físicas e químicas
Propriedades da matéria
Conclusão e exercícios sugeridos
Compreender os estados físicos da matéria vai muito além de decorar definições. Trata-se de entender como as partículas se organizam, como a energia interfere nesse comportamento e como interpretar situações do cotidiano e questões de prova.
Como próximos passos de estudo, recomenda-se:
revisar mudanças de estado físico
resolver exercícios com gráficos
comparar questões de diferentes bancas
Exercícios sugeridos:
-
ENEM – questões sobre mudanças de estado
-
Fuvest – estados físicos e partículas
-
Provas militares – diagramas e gráficos
Esse conteúdo é uma base essencial. Dominá-lo facilita enormemente o estudo de temas como separação de misturas, termoquímica e reações químicas.

